口服抗生素仅1个疗程,肠道损伤持续4-8年:Uppsala大学14979人研究证实

近期瑞典Uppsala大学等机构联合开展的一项超大规模人群研究,纳入14979名成人、追踪8年抗生素使用与粪便宏基因组数据,首次证实:口服抗生素会显著降低肠道菌群多样性,这种伤害可持续4–8年,且仅吃1个疗程就足以留下长期痕迹。
研究怎么做?1.5万人8年追踪
这项研究整合瑞典三大人群队列(SCAPIS、SIMPLER、MOS),依托瑞典处方药登记系统,精准获取受试者8年内口服抗生素处方记录,同时检测粪便宏基因组,评估肠道菌群组成。研究将抗生素暴露分为3个时间窗:近期(采样前<1年)、中期(1–4年)、远期(4–8年),系统分析抗生素对菌群的即时与长期影响。
核心发现:伤害持续4-8年,3类抗生素最危险
菌群多样性显著下降,越近伤害越大。抗生素使用与肠道菌群α多样性降低显著相关:采样前<1年使用,伤害最强;1–4年、4–8年使用,仍可检测到显著关联。简单说,4年前吃的抗生素,今天还在影响你的肠道。
3类抗生素杀伤力最大,一个疗程就中招。在11类抗生素中,克林霉素、氟喹诺酮类、氟氯西林影响最突出:1个疗程克林霉素,可让肠道物种数平均减少47种;氟喹诺酮类、氟氯西林分别减少约20种;即便是4–8年前仅用1个疗程,也与菌群多样性下降显著相关。
菌群恢复极慢,2年后几乎停滞。功能模型显示:肠道菌群在抗生素暴露后前2年恢复较快,但2年后恢复速率大幅放缓,初始损伤越重,完全复原越难。
关联代谢病、炎症,埋下健康隐患
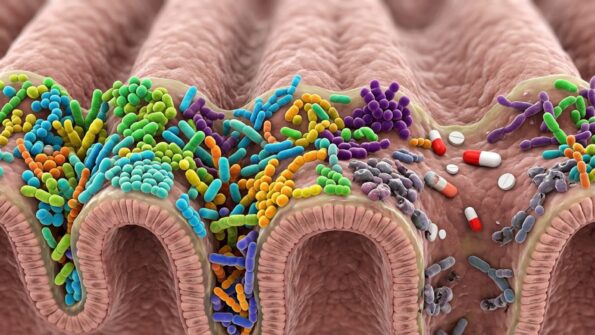
被抗生素改变的菌群中,多种细菌与高BMI、高甘油三酯、2型糖尿病、炎症相关:有害菌如活泼瘤胃球菌、迟缓埃格特菌丰度上升;有益菌如普通拟杆菌、内脏臭气杆菌丰度下降。研究者提示,这可能是抗生素长期使用与糖尿病、心血管病、结直肠息肉相关的重要机制。
女性、年轻人更易受影响。分层分析显示:女性对氟喹诺酮类、氟氯西林的菌群扰动更敏感;年轻人在克林霉素、氟喹诺酮类暴露后,物种丰度变化更显著。
机制:抗生素为何伤肠久不愈
通俗理解:1. 快速杀灭大量共生菌,物种多样性暴跌;2. 有益菌耗竭,致病菌、耐药菌趁机占位;3. 肠道生态结构被改写,恢复周期以年计算;4. 代谢、免疫、炎症通路受牵连,提升慢病风险。
守护肠道菌群:这样用抗生素更安全
研究给出实用建议:能不用就不用——病毒感冒(流涕、咽痛)无需抗生素;优先选温和款——青霉素V、广谱青霉素对菌群冲击更小;避免滥用3类重武器——克林霉素、氟喹诺酮类、氟氯西林,非必要不首选;用药后科学修复——可在医生指导下补充益生菌、多吃膳食纤维,加速菌群恢复。
研究原文发表于相关高水平期刊,样本量大、追踪时间长,为”抗生素非随意使用”提供了扎实的人群证据。核心结论:口服抗生素对肠道菌群的损伤,以年为单位计算恢复时间;克林霉素、氟喹诺酮类、氟氯西林是三大重灾区;女性和年轻人尤其需要谨慎。